はじめに
今回は同素体について、話を進めて行こう。
動画での解説はこちらを参照ください↓↓↓
ポイント1:同素体について理解しよう
まずこちらを見てもらいたい。鉛筆とダイヤモンドだ。

実はこの鉛筆の芯とダイヤモンド。同じ元素からなっているのを、諸君は知っていたか。
そう鉛筆の芯とダイヤモンドは炭素C原子から出来ている。
鉛筆だったら字が書けるが、ダイヤモンドだったら字はかけない。
一方で、これを逆に使っている人もいないだろう。
ダイヤモンドで字を書く生徒を見たことがないし、婚約指輪として鉛筆の芯を指にはめている大人を私はみたことがない。
そうなんだ。性質が明らかに違うのだ。
今日は今から、同じ元素から出来ているけど、こうして性質が違うものを見ていくことにする。
さて、この鉛筆とダイヤモンドの関係を化学の世界では、「同素体」という。
同素体とは、「同じ元素からなる単体で性質の異なるもの」のことを言うんだ。

化合物ではなく単体であることに気を付けておいてほしい。
そして、SCOPということで、同素体を持つ有名な元素がある。
それが、S硫黄、C炭素、O酸素、Pリンなのだ。
まずは、定義と共にしっかりと覚えてもらいたい。
ポイント2:それぞれの同素体の特徴を覚えよう
さぁ、今からSCOPに代表される、それぞれの同素体を見ていこう。
まずは、硫黄Sからだ。硫黄の同素体として3つを紹介したい。

1つ目が斜方硫黄だ。常温で最も安定していて、一般的な硫黄はこの斜方硫黄のことを指している。
これを加熱して溶かした後に結晶化させると、単斜硫黄と呼ばれるものになる。単斜硫黄は細長い針状の結晶だ。
斜方硫黄を加熱し続けると、液体の状態から、一度黒いドロッとした固体に変化する。そこからさらに加熱すると、黒い液体に変化する。この液体を水の中に流し込んで、急速に冷却すると、ゴム状の伸び縮みする弾性を持った物体になるのだ。それが、ゴム状硫黄だ。この3種類が硫黄の同素体だ。
次は炭素の同素体だ。
まずはこれだ。鉛筆の芯だ。これには黒鉛という名前があるから、きちんと覚えてもらいたい。
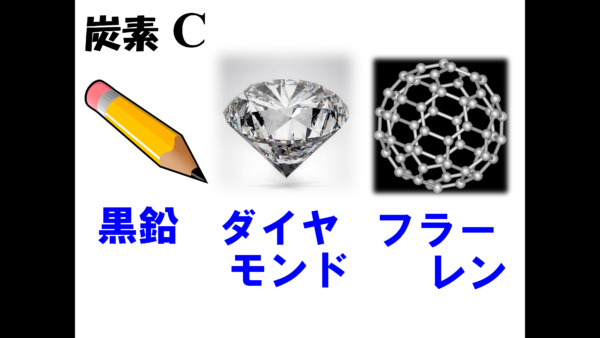
次がダイヤモンドだ。ダイヤモンドはとても硬いが電気は通さないのに対して、黒鉛は柔らかいが電気をよく通す。こちらを見てもらいたい。
黒鉛で出来たシャープペンシルの芯に電気を流してみたところだ。白熱電球を実用化した発明王のトーマス・エジソンはフィラメントの素材として京都府八幡市の竹を利用したと言われている。この2つの性質の違いと共に黒鉛とダイヤモンドは押さえてもらいたい。そしてもう一つ、フラーレンというものがある。炭素原子60個が結び付いたサッカーボール状の球体だ。フラーレンは建築家のバックミンスターフラーがデザインしたドームの形状に似ていることから、その名がついた。そして、飯島澄男 Sumio Iijimaさんがフラーレンの生成作業中に発見したと言われるカーボンナノチューブも立派な炭素原子の同素体だ。
それでは続いて、SCOPのO、酸素の同素体だ。
まずはみんなが吸って吐いている無色無臭の酸素だ。そして、酸素から出来た単体はもう一つあるのだ。それが酸素原子3つが結合したオゾンだ。
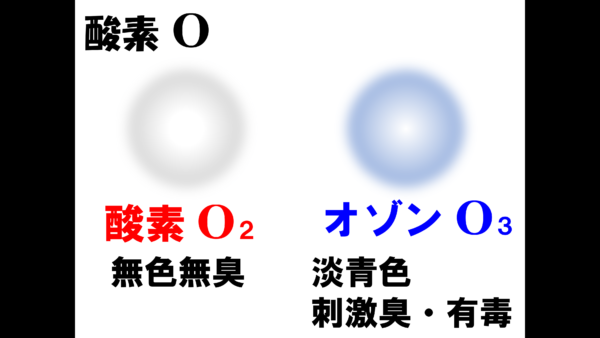
オゾンはうっすらと青い、淡青色の気体である。地球の表面に存在するオゾン層は、太陽から降り注ぐ有害な紫外線を吸収して我々の身を守ってくれる訳だが、オゾン自体は生臭く特徴的な刺激臭を持つ、我々にとって有毒な物質であるから注意してほしい。ちなみにオゾンという名称は、ギリシャ語の「臭い」を意味する言葉に由来している。
そして最後はSCOPのP、リンだ。
まずは、赤リンだ。マッチの側薬の原料として利用されている毒性のない物質だ。マッチ棒の先端も赤いがこちらではない。

紛らわしいから注意してくれ。そして、黄リンだ。黄色いリンだが、キリンではない。黄リンは強い毒性を持ち、空気中で自然発火してしまうから、水中に保存しておかないといけないのだ。
リンの危険性はこちらの動画をみるがいい!
ここで整理しておこう。

同素体を持つ元素はSCOPだ。
Sの硫黄には、斜方硫黄、単斜硫黄、ゴム状硫黄があるんだったなぁ。
Cの炭素には、黒鉛、ダイヤモンド。とりあえずこの2つを覚えておいてもらえば十分だ。余裕があれば、フラーレンやカーボンナノチューブなども知っておくとよい。そして、
Oの酸素には、酸素とオゾンがあり、
Pのリンには、赤リンと黄リンがある。
ポイント3:同素体の問題になれよう
さて、ここで問題を一つやっておこうではないか。
(1)ダイヤモンドとグラファイト(黒鉛)
(2)鉄の赤さびと黒さび (3)酸素とオゾン
(4)斜方硫黄とゴム状硫黄 (5)黄リンと赤リン
答えは(2)の鉄の赤さびと黒さびだ。今、同素体について学習した君たちなら簡単だろう。
しかし、実際の危険物の試験に出題されたものだから、しっかりと得点源にしておこう。
ちなみに赤錆は化学式で表すとFe2O3となる。その名のとおり、錆自体が赤みがかっているもので、鉄そのものを腐蝕させ、ボロボロにしていく性質を持っている。錆といった時に、まず思いつくのがこの赤錆だ。一方、黒錆は化学式で表すとFe3O4で表記され、一般的な鉄に対して自然に発生することのない、鉄の表面にできる酸化膜だ。表面に黒錆ができると、赤錆の発生を抑えることができる。このため良性の錆といわれることもある。意図的に鉄の表面に膜をつくってやり、その膜で赤錆から保護するという原理になる。
それでは、今日の講義はここまでとしておこう。それでは、皆の検討を祈る。
■その他の講義はこちらのガイドを活用ください↓